Aos 30 anos, cabeleireira passou por uma cirurgia de transposição uterina, técnica inovadora desenvolvida no Brasil cujo objetivo é preservar a fertilidade após tratamento oncológico
Por Fernanda Bassette, da Agência Einstein
A cabeleireira catarinense Angélica Hodecker era recém-casada e tinha apenas 30 anos quando recebeu o diagnóstico que a tirou o chão: ela estava com câncer de colo de útero, o terceiro tumor maligno mais frequente entre as mulheres, atrás somente dos tumores de mama e colorretal, segundo o Instituto Nacional de Câncer (INCA). Jovem e ainda sem filhos, ela queria ser mãe e se viu diante da necessidade de tomar decisões urgentes, que poderiam mudar o sonho da maternidade.
O primeiro tratamento proposto era bastante radical para uma mulher que desejava engravidar em algum momento: retirar o útero, as trompas e os ovários para eliminar qualquer chance de o câncer progredir. Com isso, teria fim o sonho de gestar. “A doença só tinha afetado o colo do útero, por que era preciso tirar tudo?”, perguntava-se a cabeleireira.
Angélica procurou um segundo especialista e chegou a outra alternativa de tratamento para seu caso: fazer uma conização, um tipo de cirurgia que retira somente a parte do colo do útero doente, preservando assim os outros órgãos do aparelho reprodutivo. A partir de então, o médico iria avaliar se era necessário ou não fazer uma intervenção mais agressiva.
Ela fez o procedimento, mas os resultados indicaram que somente a cirurgia não foi o suficiente para eliminar o tumor — seria necessário passar por quimioterapia e radioterapia pélvica. Como consequência, ela ficaria infértil.
Nesse caso, a preservação da fertilidade poderia ser feita por meio do congelamento de óvulos, mas uma futura gestação teria de ser feita em uma barriga de substituição, pois o útero que recebe radioterapia perde a elasticidade das fibras musculares e sua parte funcional, o endométrio, entra em cicatrização. Dessa forma, o órgão fica incapaz de manter uma gestação.
“A minha alternativa era interromper o tratamento de câncer para tentar engravidar o mais rápido possível. E, após a gestação, eu retomaria o tratamento contra a doença”, conta. “Descartei essa hipótese de cara. Eu queria ser mãe, mas era inviável parar o tratamento para tentar engravidar. E se o câncer progredisse nesse período?”
Foi nessa fase de incertezas que Angélica procurou uma terceira opinião. A alternativa apresentada foi fazer uma traquelectomia (procedimento que remove o colo do útero, mas não o corpo do útero) e uma linfadectomia (retirada dos gânglios da pelve).
O problema é que, mesmo após essa cirurgia, ela teria de fazer ciclos de radioterapia e quimioterapia e, consequentemente, ficaria infértil. Foi então que ela conheceu uma técnica ainda experimental, mas bastante promissora: fazer uma cirurgia de transposição uterina, ou seja, mudar o útero de lugar provisoriamente, com o objetivo de preservar o órgão para uma gravidez futura.
A proposta inédita
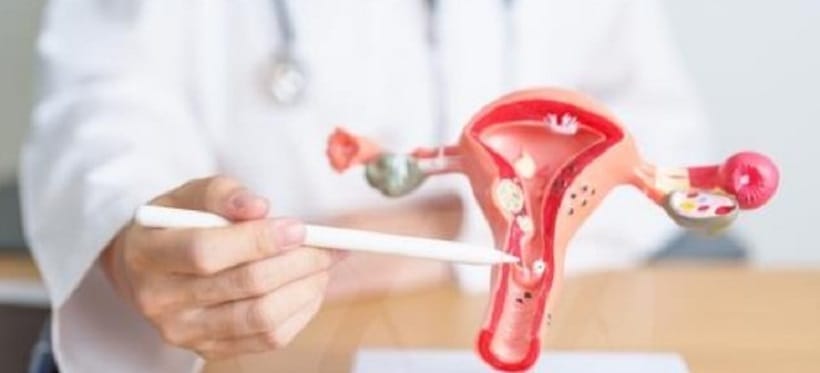
A técnica foi desenvolvida em 2015 pelo cirurgião oncológico Reitan Ribeiro, de Curitiba, e consiste em transferir os órgãos reprodutivos (útero, trompas e ovários) de lugar, reposicionando-os na parte de cima do abdômen da mulher, entre o fígado e o umbigo. A ideia é mantê-los intactos e longe dos efeitos da radiação durante o tratamento contra o câncer. Ao término dos ciclos de quimio e radioterapia, uma nova cirurgia recoloca os órgãos em sua posição original.
A proposta era fazer algo absolutamente inédito. Naquela ocasião, em 2021, outras cinco cirurgias de transposição uterina por câncer ginecológico já haviam sido feitas no Brasil, mas nenhuma delas envolvia uma paciente com câncer de colo de útero – o caso de Angélica seria o primeiro na literatura científica mundial. Até hoje, cerca de 20 mulheres fizeram essa cirurgia no Brasil.
“Estamos em um momento de transição. Partimos do conceito da cirurgia, que foi feita inicialmente de forma experimental, mas estamos constatando que ela é uma alternativa cirúrgica factível, de baixo custo e baixa complexidade, para a preservação da fertilidade nessas mulheres”, explica o ginecologista especializado em cirurgia robótica e câncer ginecológico Renato Moretti, do Hospital Israelita Albert Einstein, um dos poucos centros aptos a fazer a transposição uterina no Brasil.
“Eu não tinha nenhum comparativo, não tinha ninguém para me dizer se daria certo ou não. Havia um caso de sucesso, que resultou em gravidez, mas era um lipossarcoma [câncer raro, nas células de gordura]. Eu e meu marido pensamos muito, mas o não [não conseguir engravidar] a gente já tinha. Uma única sessão de radioterapia pélvica afetaria minha fertilidade, então decidimos tentar”, lembra Angélica, que foi paciente de Moretti nesse processo.
Mas nem todas as mulheres com câncer ginecológico são elegíveis para a cirurgia. A técnica é indicada apenas para aquelas que têm potencial de engravidar posteriormente, desejo de gestar e que a doença oncológica não acometa o útero. “Importante destacar também que a transposição uterina é de aplicabilidade imediata após a discussão multidisciplinar, com o mínimo de retardo da radioterapia que a paciente necessita para tratar o câncer”, frisa Moretti.
De acordo com o especialista, cerca de 20% a 30% das pacientes que descobrem o câncer de colo de útero nos estágios iniciais terão de ser submetidas à radioterapia pélvica. Nas fases mais avançadas, todas precisam desse tratamento. “Resumindo, a radioterapia faz parte do tratamento de câncer em pelo menos 80% das mulheres, porque a realidade do Brasil é fazer o diagnóstico em estágios mais avançados”, observa.
Angélica e o marido concordaram em tentar a transposição uterina, mas estavam preparados para o pior. Caso a técnica não funcionasse como previsto, eles fariam o congelamento de óvulos e de esperma para uma futura barriga solidária ou poderiam optar pela parentalidade via adoção. “A gente ficou um pouco com um pé atrás, porque era uma pesquisa e, se não desse certo, voltaríamos à estaca zero. Mas tínhamos que tentar.”
Em uma semana, Angélica estava no centro cirúrgico. A cirurgia foi considerada um sucesso e, em menos de 10 dias, a cabeleireira já estava no hospital para iniciar os ciclos de radioterapia. Fez todo o tratamento (25 sessões de radioterapia diariamente e seis de quimioterapia uma vez por semana) e, em março de 2021, recolocou seus órgãos no lugar.
A surpresa da gravidez espontânea
Após a cirurgia, Angélica passou a fazer um acompanhamento periódico a cada três meses para se certificar de que o câncer estava eliminado. “Tudo estava indo muito bem. O meu útero estava íntegro, vascularizado, eu estava ovulando normalmente, mas minha menstruação estava bloqueada por anticoncepcionais. Nesse período, o médico permitiu suspender o uso do anticoncepcional e falamos sobre a possibilidade de gestação”, conta.
Mas tinha mais um detalhe. Por conta do tratamento, o canal do colo uterino de Angélica estava estreitado. Seria preciso passar por um procedimento de abertura dessa região e, talvez, uma gestação natural seria mais difícil de acontecer. Moretti conversou com o casal sobre a possibilidade de uma fertilização in vitro (FIV).
“Eu era recém-casada, queria ser mãe, só que não necessariamente naquele momento. Mas quando dizem para uma mulher ‘ou você tem um bebê agora, ou talvez tenha dificuldade de engravidar futuramente’, o reloginho anda. Então engatamos a ideia de gestação logo depois do tratamento de câncer”, relata.
A proposta era tentar engravidar naturalmente no período de um ano. Se não desse certo, o casal partiria para a reprodução assistida. Não foi preciso. Cinco meses depois, Angélica engravidou sem qualquer tratamento auxiliar. “Quando minha menstruação atrasou e o primeiro teste de farmácia deu positivo, fiquei incrédula. Chorei sentada no chão do banheiro. Repeti o teste da fitinha três vezes, fiz outro digital e ainda colhi um exame de sangue para ter certeza de que era verdade”, lembra.
Ela mandou a foto do exame de farmácia para Moretti e perguntou: “Estou grávida, e agora?” E ele respondeu: “Agora vamos começar o pré-natal.” E foi assim que começou o acompanhamento da gestação inédita, mas considerada de alto risco porque ela não tinha o colo do útero.
Tudo transcorreu normalmente. Isabel – carinhosamente chamada de Bebel – nasceu na véspera de Natal, no dia 24 de dezembro de 2022, saudável, pesando 2,2 kg e medindo 43 cm. Esse nascimento foi tão importante para a literatura científica que um relato de caso foi publicado em agosto de 2024 no Journal of Surgical Oncology.
A história de Angélica abre portas para que outras mulheres com câncer ginecológico possam ser submetidas ao procedimento para preservar a fertilidade. “Foi mágico. Não quero romantizar a maternidade, mas cheguei a pensar que não poderia viver isso um dia”, diz a mãe de Bebel.
Fonte: Agência Einstein